新闻资讯
2026年2月25日福建医科大学沈祖成团队在《Molecular Psychiatry》发表了题为“Dual regulatory roles of CPT1C in chronic stress-induced depression-related outcomes”的科学研究,揭示了CPT1C通过协同调控GluA1的蛋白质合成及膜转运介导MDD发生发展的病理机制。该研究运用CRS和CUMS两种经典抑郁模型、脑立体定位注射、RiboTag及膜片钳等技术,阐明了CPT1C在MDD关键脑区伏隔核(NAc)不同神经元亚型中的差异化功能。
研究表明,慢性应激通过选择性上调NAc脑区D2-MSNs中CPT1C的表达诱导小鼠抑郁样行为发生。机制上,CPT1C能够靶向TSC2解除其对mTORC1信号通路的抑制作用,促进了GluA1蛋白质合成,并通过催化GluA1去棕榈酰化修饰促进其膜表达,增强突触传递、突触可塑性及神经元活性。此外,该研究发现D1-MSNs中CPT1C参与介导氟西汀的抗抑郁作用,揭示了该分子在不同神经元亚型中发挥相反的作用。综上,该研究揭示了CPT1C在慢性应激诱导的小鼠抑郁样行为中的双重调控机制,为抑郁症的临床治疗提供了潜在靶点及新思路。

01、慢性应激上调NAc脑区CPT1C表达水平破坏GluA1棕榈酰化稳态诱导抑郁样行为
为探究NAc脑区GluA1棕榈酰化与MDD之间的关系,作者选择构建CRS和CUMS两种经典抑郁模型,检测小鼠在慢性应激状态下NAc脑区GluA1棕榈酰化水平的变化。研究结果表明,慢性应激显著下调NAc脑区GluA1棕榈酰化水平,并显著上调GluA1表达及膜表达水平,且膜表达与棕榈酰化水平呈明显负相关。此外,作者通过显微注射棕榈酰化抑制剂2-BP抑制NAc脑区GluA1棕榈酰化修饰,显著增加了小鼠在悬尾实验(TST)和强迫游泳实验(FST)中的不动时间,成功模拟了慢性应激诱导的抑郁样行为表型,提示GluA1棕榈酰化在抑郁样行为中具有重要的调控作用。
进一步研究发现,CRS选择性上调去棕榈酰化酶CPT1C的表达,而对棕榈酰化酶DHHC3无显著影响,且CPT1C表达与GluA1棕榈酰化呈负相关、与GluA1膜表达呈正相关。基于此,研究团队利用脑立体定位注射技术过表达小鼠NAc脑区CPT1C验证其在抑郁症中的作用,实验结果显示靶点过表达后小鼠NAc脑区GluA1膜表达及总表达水平显著升高,微小兴奋性突触后电流(mEPSCs)幅度及神经元活性标志物c-fos表达也明显增加,突触传递功能与神经元活性显著增强,抑郁样行为学检测发现,NAc脑区过表达CPT1C足以诱导抑郁样行为发生,具体表现为CPT1C过表达小鼠糖水偏好率显著下降、TST及FST不动时间显著增加。上述结果表明慢性应激通过选择性上调NAc脑区CPT1C表达水平破坏GluA1棕榈酰化稳态,以此诱导小鼠抑郁样行为发生。
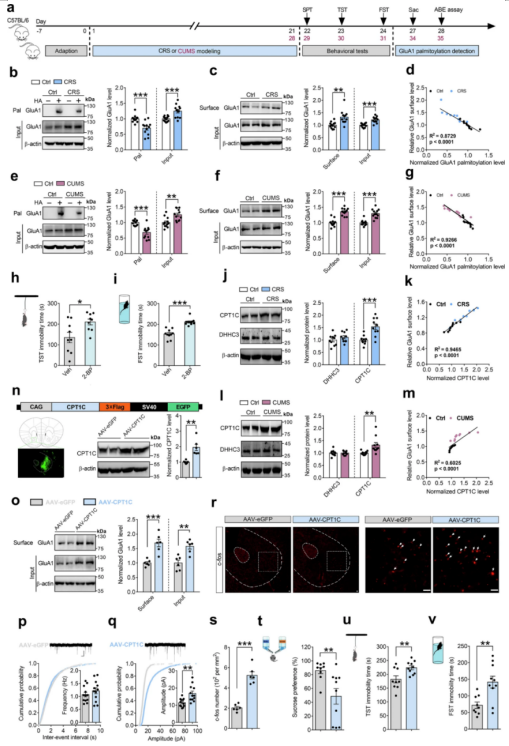
图1、CPT1C介导的GluA1棕榈酰化异常诱导抑郁样行为
02、NAc脑区D2-MSNs中CPT1C介导慢性应激诱导的小鼠抑郁样行为
NAc脑区超过95%的神经元属于中型多棘神经元(MSNs),根据受体表达类型的不同神经元可进一步细分为D1-MSNs和D2-MSNs,而两种MSNs在抑郁症中的作用相反。为进一步探究D1-MSNs和D2-MSNs中CPT1C分别对抑郁样行为的作用,该研究采用RiboTag技术分离D1-MSN和D2-MSNs,检测发现CRS选择性上调了D2-MSNs中CPT1C的mRNA及蛋白水平,而对D1-MSNs无显著影响,提示D2-MSNs中CPT1C可能在慢性应激诱导的抑郁样行为中发挥关键作用。
为印证这一结论,作者利用D2-Cre小鼠在NAc脑区中特异性过表达D2-MSNs中CPT1C,检测发现过表达小鼠GluA1棕榈酰化水平显著降低,其膜表达及总表达水平明显升高。相关性分析进一步证实,在D2-MSNs中,CPT1C表达与GluA1棕榈酰化水平呈负相关,与膜表达水平呈正相关。电生理检测发现,特异性地过表达D2-MSNs中CPT1C显著增强mEPSCs幅度,并显著提升高频刺激诱导的兴奋性突触后电位(EPSP)斜率,表明其增强了突触传递功能与突触可塑性。同时焦虑抑郁样行为学检测证实,特异性地过表达D2-MSNs中CPT1C,足以诱导小鼠出现焦虑抑郁样行为,包括减少小鼠在高架十字迷宫(EPM)开放臂和旷场实验(OFT)中心区域中的探索行为,降低糖水偏好率,并显著延长小鼠在TST和FST中的不动时间。这些结果表明D2-MSNs中CPT1C介导慢性应激诱导的小鼠抑郁样行为。
为验证靶向抑制D2-MSNs中CPT1C表达对抑郁症的治疗潜力,作者构建了Cre依赖性AAV-RNAi病毒以特异性地敲低D2-Cre小鼠NAc脑区D2-MSNs中的CPT1C表达水平。实验结果表明,特异性地敲低D2-MSNs中CPT1C有效逆转了CRS诱导的分子与功能异常,包括恢复了由CRS引起的GluA1棕榈酰化水平降低,以及抑制了由CRS引起的GluA1膜表达及总表达水平升高,并逆转了由CRS诱导的AMPAR-mEPSCs幅度增加及神经元活性标志物c-fos表达上调。
行为学结果也同样证实,该干预显著改善了CRS诱导的小鼠焦虑抑郁样行为,包括显著增加了小鼠在高架十字迷宫(EPM)开放臂和旷场实验(OFT)中心区域中的探索行为,并且显著恢复了由CRS导致的小鼠糖水偏好率降低以及在TST及FST中的不动时间增加。这些结果表明,特异性地敲低NAc脑区D2-MSNs中CPT1C可显著逆转慢性应激引起的机制异常及情绪障碍,证实CPT1C是治疗应激相关情绪障碍的潜在有效靶点。
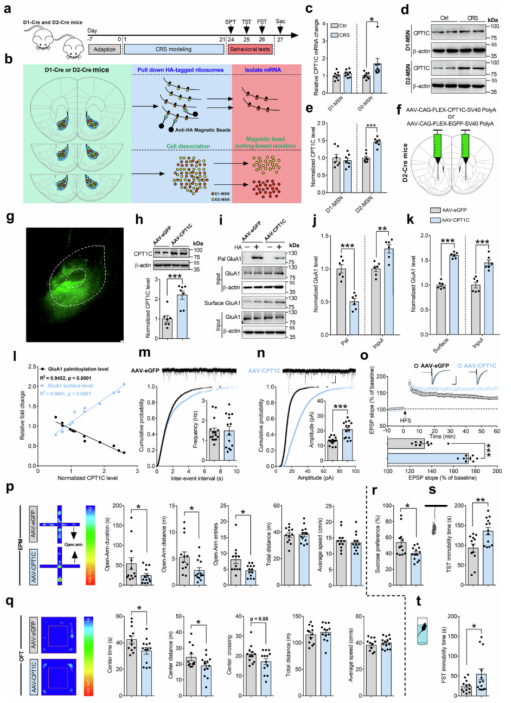
图2、D2-MSNs中CPT1C介导慢性应激诱导的小鼠抑郁样行为
03、NAc脑区D2-MSNs中CPT1C介导通过调控GluA1的蛋白质合成介导慢性应激诱导的小鼠抑郁样行为
在探究CPT1C在抑郁样行为中的作用及机制的过程中,作者发现GluA1总表达水平始终与CPT1C表达水平变化趋势一致。如在CRS和CUMS抑郁模型小鼠中,D2-MSNs中CPT1C和GluA1的表达均显著增加,且GluA1总表达与CPT1C表达呈显著正相关。而特异性地过表达NAc脑区D2-MSNs中CPT1C也重现了此趋势。这提示CPT1C可能参与调控D2-MSNs中GluA1的蛋白质合成。
为探究其机制,作者聚焦于BDNF-mTOR信号通路。特异性地敲低D2-MSNs中CPT1C可显著抑制CRS诱导的mTORC1活化及GluA1合成增加,但不影响上游的BDNF、TrkB、AKT及ERK信号。进一步研究发现,该操作逆转了CRS引起的Rheb-GTP水平升高及TSC2蛋白表达下降,且对TSC1的表达无显著性影响。以上结果表明,在D2-MSNs中,CPT1C位于BDNF/TrkB/AKT/ERK信号的下游,通过靶向TSC2解除其对下游mTORC1信号传导的抑制作用,进而促进GluA1的蛋白质合成。以上结果表明NAc脑区D2-MSNs中CPT1C还通过调控GluA1的蛋白质合成介导慢性应激诱导的抑郁样行为发生。
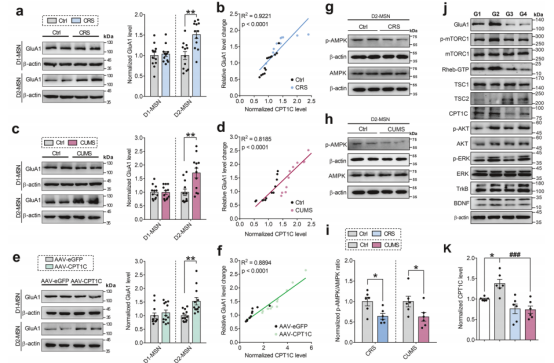
图3、NAc脑区D2-MSNs中CPT1C介导通过调控GluA1的蛋白质合成介导慢性应激诱导的小鼠抑郁样行为
04、CPT1C在D1-MSNs中的上调是氟西汀发挥抗抑郁作用的关键机制
早期研究报道D1-MSNs活性介导了氟西汀和氯胺酮的抗抑郁作用,研究团队进一步探究了D1-MSNs中CPT1C在其中的潜在机制。作者对D1-Cre和D2-Cre小鼠进行了艾司氯胺酮(10 mg/kg)或氟西汀(20 mg/kg)的腹腔注射处理,并收集NAc脑组织分析抗抑郁药对D1-MSNs及D2-MSNs中GluA1棕榈酰化水平及棕榈酰化相关酶的影响。该研究发现艾司氯胺酮单次给药2小时或24小时不影响两种神经元中CPT1C及DHHC3的表达。然而,氟西汀14天给药处理可选择性上调D1-MSNs中CPT1C的表达。
此外,特异性地敲低D1-MSNs中CPT1C能够显著逆转氟西汀诱导的D1-MSNs中GluA1的棕榈酰化水平降低、膜表达及总表达水平升高,以及AMPAR-mEPSCs幅度与频率的增强和神经元活性标志物c-fos的表达上调。行为学结果证实,下调D1-MSNs中CPT1C能阻断氟西汀的抗抑郁效应,表现为糖水偏好率重新降低,悬尾实验与强迫游泳中的不动时间增加。以上结果表明CPT1C在D1-MSNs中的上调是氟西汀发挥抗抑郁作用的关键机制,这揭示了同一分子在不同神经元亚型中可介导截然相反的病理过程及治疗作用,为开发细胞类型特异性的抗抑郁策略提供了新靶点。
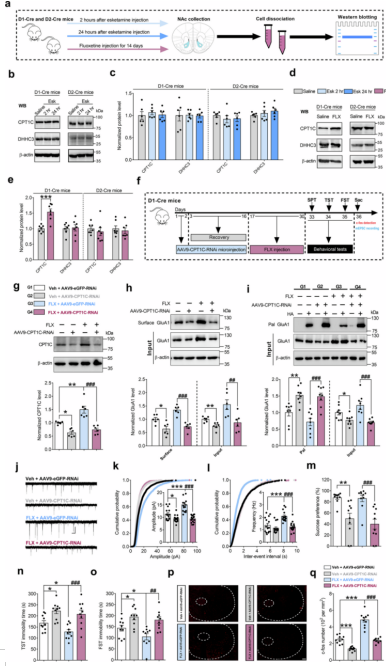
图4、CPT1C在D1-MSNs中的上调是氟西汀发挥抗抑郁作用的关键机制
本研究揭示了NAc脑区D2-MSNs中CPT1C在慢性应激诱导的抑郁样行为中的作用机制。研究结果表明,慢性应激选择性上调D2-MSNs中CPT1C的表达,进而通过双重途径协同增强AMPAR介导的突触传递及神经元活性。一方面,CPT1C通过下调TSC2解除其对mTORC1的抑制作用,促进GluA1的蛋白质合成;另一方面,CPT1C直接催化GluA1的去棕榈酰化修饰,增加其在细胞膜上的表达。这两条通路共同作用,显著增强突触传递及突触可塑性,最终驱动抑郁样行为的产生。此外,本研究还揭示了CPT1C在D1-MSNs中介导氟西汀抗抑郁作用的特异性机制,揭示该分子在不同神经元亚型中发挥相反的病理与治疗功能。
这些发现首次阐明了CPT1C通过同时调控GluA1的蛋白质合成与膜转运参与应激相关的情绪障碍进程,为理解抑郁症的发病机制提供了新视角,并为临床治疗提供了细胞类型特异性的潜在靶点。未来研究将进一步探究CPT1C在D1-与D2-MSNs功能调节中的桥梁作用及其转化价值。
参考文献:https://doi.org/10.1038/s41380-026-03516-4


想了解更多内容,获取相关咨询请联系
电 话:+86-0731-84428665
伍经理:+86-180 7516 6076
工程师:+86-180 7311 8029
邮 箱:consentcs@163.com

订购和售后

邮箱:consentcs@163.com
地址:湖南省长沙市高新技术开发区青山路699号湖南省军民融合科技创新产业园8栋B座1609室
微信公众号
Copyright © 康森特生物科技(长沙)有限公司 2024
本网站销售的所有产品均不得用于人类或动物之临床诊断或治疗,仅可用于工业或者科研等非医疗目的。

售前:+86-0731-84228665
+86 -180 7516 6076
售后:+86 -180 7516 7741
传真:+86-0731-84228665


